第25届全国临床肿瘤学大会暨2022年中国临床肿瘤学会(CSCO)学术年会今日正式拉开帷幕,北京、上海、广州、济南、哈尔滨五大会场采用线下线上相结合的方式同步举行,大会汇聚了中国临床肿瘤学最前沿,临床研究最具影响力的科研成果。翰森制药创新药阿美乐®(甲磺酸阿美替尼片)四篇临床研究数据在本届年会上权威发布。
阿美乐®(甲磺酸阿美替尼片)是由翰森制药自主研发的首个中国原创三代EGFR-TKI创新药,也是全球首个中位无进展生存期(mPFS)超过1年(二线使用)的三代 EGFR-TKI。其在既往经EGFR-TKI治疗时或治疗后出现疾病进展的,存在EGFR T790M突变阳性的局部晚期或转移性NSCLC成人患者治疗方面疗效显著。
因其优异的疗效与安全性,阿美乐®(甲磺酸阿美替尼片)已多次亮相国内外学术会议。2022 CSCO年会正式发布了阿美替尼在非小细胞肺癌(NSCLC)脑(膜)转移治疗、辅助治疗、T790M阴性、靶向联合治疗方向上的四大最新临床研究。
01. 摘要介绍
阿美替尼治疗初诊或复发的脑/脑膜转移非小细胞肺癌(NSCLC)的剂量探索研究(ARTISTRY)
作者:王慧娟 河南省肿瘤医院
ARTISTRY研究(NCT04778800)旨在观察不同剂量阿美替尼对EGFR突变NSCLC脑/脑膜转移患者的疗效和安全性,其队列1中脑实质转移患者接受阿美替尼110mg/d一线治疗,当患者仅颅内进展而其余部位未进展时,阿美替尼剂量递增至165mg。
本次会议报告了ARTISTRY研究的脑实质转移队列的主要疗效和安全性数据。截至2022年3月,共纳入14例脑实质转移患者,每天给予阿美替尼110mg治疗,其中有3例患者加量至165mg,其中12例纳入CNS全分析集(cFAS),10例患者纳入CNS可评估响应集(cEFR)。iPFS和PFS尚未成熟,iORR为66.7%和80.0%。cFAS和cEFR的iDCR均为100%。165mg组iDCR为100%(3/3)。整体安全性良好,未见3级以上不良事件。
ARTISTRY研究初步证实,阿美替尼作为EGFR突变NSCLC脑转移患者的一线治疗药物,具有优异的抗肿瘤活性和可控的安全性。
02. 摘要介绍
阿美替尼作为EGFR突变阳性非小细胞肺癌术后辅助治疗
作者:胡坚 浙江大学医学院附属第一医院
截至2022年1月,本研究共纳入66例Ⅰ-Ⅲ期、具有EGFR突变阳性(19Del或L858R)、经过根治手术后的非小细胞肺腺癌患者。每天给予阿美替尼110mg,根据病理分期和患者身体状况给予6~36个月的用药时间,以此评估患者的无病生存期(DFS)、安全性和耐受性。所有患者病情稳定,未发生肿瘤复发和CNS转移,患者1年DFS率达100%。无≥3级不良反应发生,安全性优势明显。
这项研究首次证明了阿美替尼作为辅助治疗药物对于完全切除、Ⅰ-Ⅲ期伴有EGFR突变的NSCLC患者具有显著疗效且安全性良好。目前,该研究仍在进一步分析中,2年DFS率、中位DFS等其他长期生存结果会在后续会议中陆续公布。
03. 摘要介绍
阿美替尼二线治疗EGFR T790M突变阴性晚期非小细胞肺癌的疗效及安全性
作者:龙皆然 北京肿瘤医院
2021年12月,本研究回顾性分析12例EGFR敏感突变阳性、已接受过一/二代EGFR-TKI治疗并出现疾病进展NSCLC患者的临床资料,所有患者均经检测确认为T790M突变阴性,并接受阿美替尼(110mg,口服,每天一次)治疗。
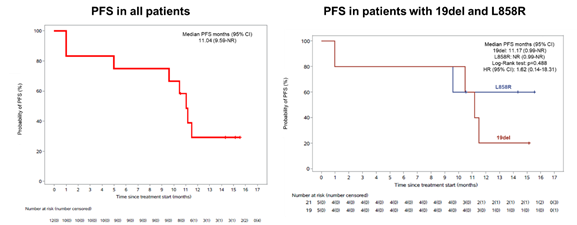
中位随访时间为15.6个月,ORR为16.7%(2/12; 95%CI:2.1%-48.4%),DCR为83.3%(10/12; 95% CI:51.6%-97.9%),中位PFS为11.0个月(95% CI: 9.6-NR),19del和L858R人群的中位PFS无统计学差异(11.2vs.NR月,HR=1.62, P=0.488)。
4名患者发生治疗相关不良事件(TRAE),其中皮疹(3/12; 25%)和腹泻(3/12; 25%)最常见,根据CTCAE v5.0均为1级。
该项研究证实阿美替尼在一/二代EGFR-TKI治疗后耐药的EGFR T790M突变阴性晚期NSCLC患者中具有较好的抗肿瘤作用以及良好的安全性。
04. 摘要介绍
阿美替尼联合安罗替尼一线治疗EGFR突变NSCLC
作者:陈华林 广东医科大学附属医院
截至2022年3月,本研究共纳入了11例未经治疗的晚期EGFR突变NSCLC患者,其中脑转移7例(63.6%)。具体治疗方案是阿美替尼110mg/d联合安罗替尼12mg/d治疗,直至出现不可耐受的毒性和肿瘤进展。
11例患者均达到PR,总体ORR为100%(11/11);7例脑转移患者接受颅内靶病灶评估,其中5例达到PR,2名SD,iORR为71.4%(5/7),iDCR为100%(7/7)。没有患者因不良反应停药,安全性良好。
本研究计划入组63例,目前研究正在持续开展中。此次初步结果展示了阿美替尼联合安罗替尼一线治疗EGFR突变NSCLC优秀的ORR数据,且安全性可控。结果提示,阿美替尼联合安罗替尼方案可能是一线治疗EGFRm+NSCLC的优秀选择。
您可登录以下网址查看2022 CSCO年会入选摘要详细信息:
http://csco.kydev.net/poster/cxzc
阿美替尼相关研究将于会议召开期间公布包含更多信息的Poster,敬请期待!
